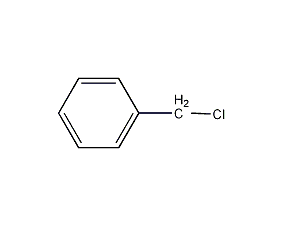
结构式
| 物竞编号 | 02HX |
|---|---|
| 分子式 | C7H7Cl |
| 分子量 | 126.59 |
| 标签 |
苄 基 氯;α -氯 甲 ;, 1-Chloromethylbenzene,α -Chlorotoluene, 芳香族卤素衍生物 |
编号系统
CAS号:100-44-7
MDL号:MFCD00000889
EINECS号:202-853-6
RTECS号:XS8925000
BRN号:471308
PubChem号:暂无
物性数据
1.性状:无色至黄色液体,有不愉快的刺激性气味。[1]
2.熔点(℃):-48~-39[2]
3.沸点(℃):175~179[3]
4.相对密度(水=1):1.10[4]
5.相对蒸气密度(空气=1):4.36[5]
6.饱和蒸气压(kPa):2.93(78℃)[6]
7.燃烧热(kJ/mol):-3705.2[7]
8.临界压力(MPa):3.91[8]
9.辛醇/水分配系数:2.3[9]
10.闪点(℃):67(CC);74(OC)[10]
11.引燃温度(℃):585[11]
12.爆炸上限(%):14[12]
13.爆炸下限(%):1.1[13]
14.溶解性:不溶于水,可混溶于乙醇、氯仿、等多数有机溶剂。[14]
15.黏度(mPa·s,20ºC):1.38
16.黏度(mPa·s,30ºC):1.175
17.蒸发热(KJ/mol,25ºC):51.1
18.相对密度(20℃,4℃):1.0127
19.常温折射率(n25):1.538920
20.相对密度(25℃,4℃):1.089830
21.溶度参数(J·cm-3)0.5:20.123
22.van der Waals面积(cm2·mol-1):8.450×109
23.van der Waals体积(cm3·mol-1):67.690
24.气相标准声称热(焓)( kJ·mol-1) :18.9
25.液相标准声称热(焓)( kJ·mol-1):-32.6
26.液相标准热熔(J·mol-1·K-1):187.4
毒理学数据
1.急性毒性[15]
LD50:1231mg/kg(大鼠经口)
LC50:778mg/m3(大鼠吸入,2h)
2.刺激性 暂无资料
3.致突变性[16] 微生物致突变:鼠伤寒沙门菌600μmol/皿;大肠杆菌10mg/L。微生物致突变:鼠伤寒沙门菌7900nmol/皿。DNA损伤:人成纤维细胞1mmol/L。程序外DNA合成:人类Hela细胞50μmol/L。微核试验:仓鼠胚胎1μmol/L。姐妹染色单体交换:仓鼠卵巢100μmol/L。
4.致癌性[17] IARC致癌性评论:G2A,可能人类致癌物。
生态学数据
1.生态毒性[18]
LC50:6mg/L(96h)(黑头呆鱼,静态);4mg/L(96h)(斑马鱼,静态);1.9mg/L(96h)(青鳉)
EC50:3.2mg/L(48h)(水蚤)
2.生物降解性[19]
好氧生物降解(h):168~672
厌氧生物降解(h):672~2688
3.非生物降解性[20]
空气中光氧化半衰期(h):22~218
一级水解半衰期(h):15
分子结构数据
1、摩尔折射率:36.01
2、摩尔体积(cm3/mol):117.1
3、等张比容(90.2K):282.5
4、表面张力(dyne/cm):33.8
5、极化率:14.27
计算化学数据
1.疏水参数计算参考值(XlogP):无
2.氢键供体数量:0
3.氢键受体数量:0
4.可旋转化学键数量:1
5.互变异构体数量:无
6.拓扑分子极性表面积0
7.重原子数量:8
8.表面电荷:0
9.复杂度:55.4
10.同位素原子数量:0
11.确定原子立构中心数量:0
12.不确定原子立构中心数量:0
13.确定化学键立构中心数量:0
14.不确定化学键立构中心数量:0
15.共价键单元数量:1
性质与稳定性
1.热水中会缓慢水解生成苄醇。芳环可以发生氯化、硝化、磺化等反应。氯甲基可以水解、氧化生成甲醇和甲酸。
2.稳定性[21] 稳定
3.禁配物[22] 强氧化剂、铁、铁盐、铝、水、醇类
4.避免接触的条件[23] 潮湿空气、受热
5.聚合危害[24] 不聚合
6.分解产物[25] 氯化氢
贮存方法
储存注意事项[26] 储存于阴凉、干燥、通风良好的库房。远离火种、热源。库温不超过30℃,相对湿度不超过70%。包装必须密封,切勿受潮。应与氧化剂、金属粉末、醇类、食用化学品分开存放,切忌混储。配备相应品种和数量的消防器材。储区应备有泄漏应急处理设备和合适的收容材料。
合成方法
1.连续光氯化法 将干燥不含铁质的加到无铁反应器中,在光照下进行高温氯化。然后分馏氯化产物,即得氯化苄,副产氯化氢用水吸收得盐酸,副产α-二氯甲基可经水解作用制成甲醛。
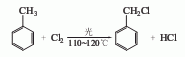
2.无光热氯化法 先静置6h以上以除去铁质,再经高位槽送入氯化锅中,以蒸气加热至沸腾后停止加热,通入氯气进行氯化,连续反应制得的氯化苄通过底部溢流管冷却后进入贮槽。氯化苄的制备主要由氯化而得。目前国内外主要有两种方法:光氯化法和无光热氯化法。从工艺操作来分,两种方法又各有间歇操作和连续操作两种。从反应器结构来分,连续操作又可分为水平连续操作和垂直连续操作两种。由于连续光氯化法具有小批量生产容易上马,反应速度比无光热氯化法快的优点,国内较多厂家采用此工艺。一般采用小型水平串联连续式反应器组。将干燥不含铁质的加入玻璃氯化瓶中,加热至110℃,使液体缓缓沸腾,按氯气与质量比为1∶2.5在日光灯照射下通入氯气,于110~120℃进行高温氯化反应至终点。蒸馏回收未反应的,收集160~180℃馏分即为粗品氯化苄。再经常压分馏,收集176~182℃馏分,即得到氯化苄成品。
无光热氯化法则一般采用大型垂直连续式搪瓷反应釜。此外,在催化剂过氧化物存在下与氯化亚硫反应,或在氯化锌催化下环氯甲基化等,均可制得氯化苄。
3.制法:
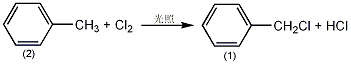
于装有温度计、回流冷凝器(顶部连一氯化钙干燥音,干燥管连接氯化氢和氯气吸收装置)、通气导管的反应瓶中,加入(2)92g(1.0mol),几粒沸石,油浴加热至沸。用一只200W的灯泡照射①,通入经浓干燥的氯气(直接通到反应瓶底部),在微沸状态下连续通氯直至瓶内温度升至156℃时,停止通氯。常压蒸馏,先回收未反应的,再收集165~185℃的馏分。重新蒸馏,收集178~182℃的馏分。得氯化苄(1)①90g,收率70%。注:①也可用日光灯或石英灯照射,该反应为自由基型反应。②也可用甲基在过氧化戊存在下与氯化亚砜反应来制备,或由的氯甲基化等反应来制备。[28]
用途
用作染料中间体及用于单宁、香料、药品等的合成。[27]




