概述[1]
由于四基氨化膦含杂原子的有机化合物在功能材料、生物医药等领域的广泛应用,对于这类化合物的合成受到了广泛的关注。四基氨化膦已被广泛用来合成胍类、脒类等重要的含氮化合物。同时,N和P虽然属于同一主族,但成键性能却有很大差异,比如四基氨化膦中N只和一个环相连,而P则同时连接三个环。考虑到N,P电负性的差异,共轭扩展的四基氨化膦衍生物可能具有特殊的光谱性质。四基氨化膦可用于钝化添加剂能形成更加稳定的界面膜,钝化正极材料表面,使材料结构不容易崩塌,减少电解液和锂盐的分解,从而提升电池的循环性能。

制备[2]
(1)向19.3g化合物a1(![]() )中加入5%的盐酸1L,反应温度控制在5℃,搅拌1h;
)中加入5%的盐酸1L,反应温度控制在5℃,搅拌1h;
(2)向上述反应溶液中加入10%的亚硝酸钠水溶液100mL,反应温度控制在5℃,搅拌1h;
(3)向上述反应溶液中加入加入8%的叠氮化钠水溶液100mL,反应温度控制在5℃,搅拌1h;经萃取、洗涤、干燥、过滤,除去溶剂,柱层析得到化合物b1,该化合物b1即为本发明的种中间体。种中间体的表征数据如下: 1HNMR(500MHz,CDCl3):δ=3.81(s,2H),6.63(d,J=8.5Hz,2H),7.27-7.35(m,5H),7.50(d,J=8.0Hz,2H);13CNMR(125MHz,CDCl3):δ=87.28,90.06,112.57,114.71,127.63,128.24,131.31,132.93,146.60;
由以上表征数据可得知种中间体的分子结构式如下:
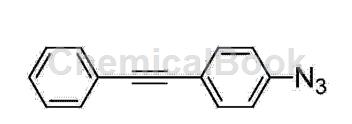
(4)在惰性气体保护下,向30.4g化合物c1(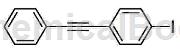 )中加入四氢呋喃3L、50mL正丁基锂(2.5M),反应温度控制在-80℃,搅拌2h;
)中加入四氢呋喃3L、50mL正丁基锂(2.5M),反应温度控制在-80℃,搅拌2h;
(5)向上述反应溶液中加入11.1g三溴化磷,反应温度控制在-25℃,搅拌2h;
(6)向上述反应溶液中加入40mL硼烷-四氢呋喃络合物(1M),反应温度控制在-25℃,搅拌2h,萃取、洗涤、干燥、过滤,除去溶剂;
(7)向上述混合物中加入2L二乙胺,反应温度控制在30℃,搅拌2h;经萃取、洗涤、干燥、过滤,除去溶剂,柱层析得到化合物d1,该化合物d1即为本发明的第二种中间体。第二种中间体的表征数据如下:1HNMR(500MHz,CDCl3):δ=7.29(t,J=8.0Hz,6H),7.35-7.37(m,9H),7.51-7.55(m,12H);13CNMR(125MHz,CDCl3):δ=87.38,90.11,122.55(d,J=7.1Hz),127.62,128.36,128.82,,132.08,132.15,135.88(d,J=19.6Hz),136.92(d,J=10.7Hz)。
(8)在惰性气体保护下,取21.9g上述制备方法制得的化合物b1和56.3g化 合物d1,混合后溶于5L中,加热回流反应10h,经萃取、洗涤、干燥、过滤,除去溶剂,柱层析得到本实施例的四基氨化膦。
本方法的四基氨化膦的化合物表征数据:UV-vis(CH2Cl2)λmax:316nm;1HNMR(500ΜΗz,CDCl3):δ=6.77(d,J=8.0Hz,2H),7.21-7.29(m,5H),7.34(t,J=7.0Hz,9H),7.46(d,J=7.0Hz,2H),7.53-7.55(m,6H),7.60-7.62(m,6H),7.69-7.74(m,6H);13CNMR(125MHz,CDCl3):δ=87.61,88.26(d,J=2.1Hz),90.86,92.45,111.56,122.43,123.25(d,J=18.1Hz),124.15,127.26(d,J=3.1Hz),127.29,128.12,128.38,128.80,129.51(d,J=99.8Hz),131.19,131.69(d,J=12.4Hz),131.72132.33(d,J=10.3Hz),132.40,151.43(d,J=2.0Hz);Anal.calcdforC56H36NP:C89.22,H4.81,N1.86;foundC89.13,H4.82,N1.92。
主要参考资料
[1] 方敬坤, 俞宪, & 杨鑫. 一种四基氨化膦衍生物及其合成方法.
[2] 万琼琼. (2007). 新型α-氨基膦酸酯及其酰胺衍生物的合成与生物活性研究. (Doctoral dissertation, 贵州大学).
[3] 王萍, 吕循峰, 刘勇, 娄勇刚, & 张郁茹. 一种锂离子电池高温电解液.




