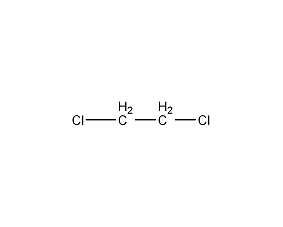
结构式
| 物竞编号 | 02UK |
|---|---|
| 分子式 | C2H4Cl2 |
| 分子量 | 98.96 |
| 标签 |
对称, 乙撑二氯, 1,2-, 二氯化乙烯, 1,2-Bichloroethane, Ethylene dichloride, Sym-Dichloroethane, Ethylene chloride, EDC;Brocide, 脂肪族卤代衍生物 |
编号系统
CAS号:107-06-2
MDL号:MFCD00000963
EINECS号:203-458-1
RTECS号:KI0525000
BRN号:605264
PubChem号:暂无
物性数据
1.性状:无色或浅黄色透明液体,有类似氯仿的气味。[1]
2.熔点(ºC):-35.7[2]
3. 沸点(ºC):83.5[3]
4.相对密度(水=1):1.26[4]
5.相对蒸气密度(空气=1):3.42[5]
6.饱和蒸气压(kPa):13.33(29.4℃)[6]
7.燃烧热(kJ/mol):-1243.9[7]
8.临界温度(℃):290[8]
9.临界压力(MPa):5.36[9]
10.辛醇/水分配系数:1.48[10]
11.闪点(℃):13[11]
12.引燃温度(℃):413[12]
13.爆炸上限(%):16.0[13]
14.爆炸下限(%):6.2[14]
15.溶解性:微溶于水,可混溶于乙醇、、氯仿和多数普通溶剂。[15]
16.临界密度(g·cm-3):0.440
17.临界体积(cm3·mol-1):225
18.临界压缩因子:0.259
19.偏心因子:0.288
20.Lennard-Jones参数(A):7.814
21.Lennard-Jones参数(K):253.6
22.溶度参数(J·cm-3)0.5:20.250
23.van der Waals面积(cm2·mol-1):6.300×109
24.van der Waals体积(cm3·mol-1):43.700
25.气相标准声称热(焓)( kJ·mol-1) :-132.84
26.气相标准熵(J·mol-1·K-1) :305.96
27.气相标准生成自由能( kJ·mol-1):-74.2
28.气相标准热熔(J·mol-1·K-1):77.32
29.液相标准声称热(焓)( kJ·mol-1):-167.99
30.液相标准熵(J·mol-1·K-1) :208.53
31.液相标准生成自由能( kJ·mol-1):-82.42
32.液相标准热熔(J·mol-1·K-1):128.9
毒理学数据
1.急性毒性[16]
LD50:670mg/kg(大鼠经口);2800mg/kg(兔经皮)
LC50:1000ppm(大鼠吸入,7h)
2.刺激性[17]
家兔经皮:625mg,轻度刺激(开放性刺激试验);
家兔经眼:63mg,重度刺激。
3.亚急性与慢性毒性[18] 猴吸入0.22g/m3,每天7h,每周5d,125次,无症状;4.11g/m3,每天7h,5d/周,25~50次,死亡率较高。
4.致突变性[19] DNA抑制:人淋巴细胞5ml/L。哺乳动物体细胞突变:人淋巴细胞100mg/L
5.致癌性[20] IARC致癌性评论:G2B,人类可疑致癌物。
6.其他[21] 大鼠吸入低中毒浓度(TCLo):300ppm(7h)(孕6~15d),引起植入后死亡率增加。LDLo:286mg/kg(人经口);TDLo:428mg/kg(人经口);TCLo:4000ppm(人吸入,1h)
生态学数据
1.生态毒性[22]
LC50:225mg/L(96h)(虹鳟鱼,静态);230~710mg/L(96h)(蓝鳃太阳鱼,静态);136mg/L(96h)(黑头呆鱼,静态);65mg/L(96h)(褐虾);218mg/L(48h)(水蚤)
IC50:105~710mg/L(72h)(藻类)
2.生物降解性[23]
好氧生物降解(h):2400~4320
厌氧生物降解(h):9600~17280
3.非生物降解性[24]
空气中光氧化半衰期(h):292~2917
一级水解半衰期(h):1.1a
分子结构数据
1、摩尔折射率:21.01
2、摩尔体积(cm3/mol):84.3
3、等张比容(90.2K):188.6
4、表面张力(dyne/cm):25.0
5、极化率:8.33
计算化学数据
1.疏水参数计算参考值(XlogP):无
2.氢键供体数量:0
3.氢键受体数量:0
4.可旋转化学键数量:1
5.互变异构体数量:无
6.拓扑分子极性表面积0
7.重原子数量:4
8.表面电荷:0
9.复杂度:6
10.同位素原子数量:0
11.确定原子立构中心数量:0
12.不确定原子立构中心数量:0
13.确定化学键立构中心数量:0
14.不确定化学键立构中心数量:0
15.共价键单元数量:1
性质与稳定性
1.在空气、水分及光照下逐渐分解,酸度增加,颜色变深。加入少量烷基胺可完全防止分解发生。加压下160~175℃水解生成乙二醇,碱性水溶液可促进水解反应。
2.在高温加热时发生热裂,生成氯乙烯和氯化氢。与强碱一起加热时也可发生脱氯化氢反应。
3.在光照或在氯化铁的催化作用下,发生液相氯化,生成1,1,2-三氯乙烷,继续氯化生成四氯乙烷等多氯衍生物。
4.该品中的氯原子富有反应性。例如与氨在加压下加热至120℃生成乙二胺;与氰化钠反应生成丁二腈;在Fridel-Crafts型催化剂存在下与反应,生成二乙烷。
5.属高毒类。对眼和呼吸道有刺激作用,其蒸气可使动物角膜浑浊,有麻醉性。能使动物皮肤产生硬结,并能引起心、肝、肾的脂肪性病变直到死亡。人口服15~20ml可致死,接触浓度为0.1g/m3时有易倦、头痛、失眠、植物神经系统功能紊乱症状,对动物有明显致癌作用。TJ36-79规定车间空气中高容许浓度为25mg/m3。
6.稳定性[25] 稳定
7.禁配物[26] 强氧化剂、酸类、碱类
8.避免接触的条件[27] 受热
9.聚合危害[28] 不聚合
10.分解产物[29] 氯化氢
贮存方法
储存注意事项[30] 储存于阴凉、通风的库房。远离火种、热源。库温不宜超过37℃。保持容器密封。应与氧化剂、酸类、碱类、食用化学品分开存放,切忌混储。采用防爆型照明、通风设施。禁止使用易产生火花的机械设备和工具。储区应备有泄露应急处理设备和合适的收容材料。
合成方法
1.乙烯与氯气直接合成法 以乙烯和氯气在1,2-介质中进行氯化生成粗及少量多氯化物,加碱闪蒸除去酸性物及部分高沸物,用水洗涤至中性,共沸脱水,精馏,得成品。
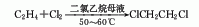
2.乙烯氧氯化法乙烯直接与氯气氯化生成。由裂解制氯乙烯时回收的氯化氢和预热至150-200℃的含氧气体(空气)和乙烯,通过载于氧化铝上的氯化铜触媒,在压力0.0683-0.1033MPa;温度200-250℃下反应,粗产品经冷却(使大部分三氯乙醛和部分水冷凝);加压;精制,得产品。
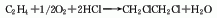
3.由石油裂解气或焦炉的乙烯直接氯化的方法。此外,在氯乙醇;环氧乙烷的生产中还副产有1,2-。
4.将工业品1,2-是用浓洗至酸层无色,而后用5%的氢氧化钙溶液洗,再用水洗一次,分去水层。用无水氯化钙干燥后,进行精馏。1,2-能与水形成共沸混合物,含有8.9%的水,共沸点7.7℃。利用此特性脱去大量的水后再进行干燥和蒸馏即得纯品1,2-。
5.将催化剂三氯化铁、氯化铜或氯化亚锑悬浮于中作为反应介质,分别通入气体乙烯和氯气进行反应,控制反应温度为50~70℃,反应压力0.4~0.5 MPa:
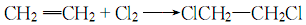
反应所得产物用水洗去氯化氢和催化剂,静置分层,分去水层,然后用1%~2%的氢氧化钠洗涤,分去水层后进行共沸精馏,蒸出的共沸物静置分去水层,干燥后,再精馏,即得1,2-纯品。
用途
1.主要用作氯乙烯;乙二醇;乙二酸;乙二胺;四乙基铅;多乙烯多胺及联甲酰的原料。也用作油脂;树脂;橡胶的溶剂,干洗剂,农药除早菊素;咖啡因;维生素;激素的萃取剂,湿润剂,浸透剂,石油脱蜡,抗震剂,还用于农药制造以及药物灭虫宁;哌哔嗪的原料。在农业上可用作粮食;谷物的熏蒸剂;土壤消毒剂等。
2.用于硼的分析,油脂及烟草的萃取剂。也用于乙酰纤维素的制造。
3.用作分析试剂,如作溶剂、色谱分析标准物质。还用作油脂的萃取制,并用于有机合成。
4.作洗涤剂、萃取剂、农药和金属脱油剂等。
5.用作蜡、脂肪、橡胶等的溶剂及谷物杀虫剂。[31]




