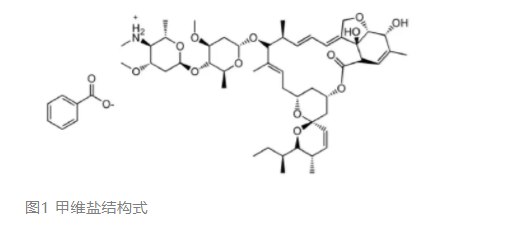
甲氨基阿维菌素甲酸盐的抗性机理研究进展甲氨基阿维菌素甲酸盐 (emamectin benzoate),简称甲维盐,结构式见图1,是1984年美国默克公司对4″-(α-1-齐墩果糖基)-α-1-齐墩果糖上的羟基进行衍生化研究的结果。甲维盐作为一种新型抗生素类生物源杀虫剂,具有广谱、高效、低毒、低残留等优点,对鳞翅目害虫具有良好的杀虫效果,甲维盐对一些鳞翅目昆虫的LC90值范围在0.002~0.89 mg/L。与其先导化合物阿维菌素相比较,甲维盐的毒性更低,对大鼠的毒性仅为阿维菌素的1/6,常规剂量下对人、畜等安全,且易降解。
在过去的几十年里,由于新型杀虫剂甲维盐具有独特的作用方式,且对鳞翅目害虫幼虫表现出很好的毒性,如小菜蛾、菜青虫等重要蔬菜害虫,尤其对小菜蛾、甜菜夜蛾有特效,同时对螨类害虫有较高活性,我国引入其来控制鳞翅目害虫的危害,初应用于甘蓝、白菜和萝卜等蔬菜上防治小菜蛾,后逐步推广到经济作物,乃至大田作物。其在防治效果上对很多害虫显示出其他农药无法比拟的活性:对小菜蛾、甜菜夜蛾、二化螟和朱砂叶螨的相对毒力分别是阿维菌素的10.54、10.50、1.50、0.69,对亚热带黏虫的毒力比灭多威、硫双威和氰戊菊酯毒力高1720、884、268倍,对鳞翅目害虫杀虫活性比阿维菌素高1500倍,如甜菜夜蛾,对灰翅夜蛾、烟草夜蛾及谷类夜蛾的胃毒毒力分别是阿维菌素的1166、43、105倍。

尽管我国鳞翅目害虫对阿维菌素类杀虫剂抗药性的发展还没有引起明显的田间防治失败,大规模的阿维菌素类杀虫剂抗性暴发还未出现,但是近年的研究和田间抗性监测发现,部分蔬菜害虫已经对其产生了抗性,且抗药性有逐步升高的趋势。所以必须高度重视这一潜在风险,以防防治失败造成作物大面积减产甚至绝收。为了延缓害虫对甲维盐抗药性的产生及发展,延长其使用寿命,必须对其作用机制、抗性现状和抗性机理进行深入研究。
1.甲维盐抗性发展研究概况
目前,甲维盐/阿维菌素常用于防治蔬菜害虫,如小菜蛾、甜菜夜蛾、斜纹夜蛾等,由于其防治效果良好,在十字花科蔬菜害虫防治上得到广泛应用且有效控制了鳞翅目害虫种群的发生规模,延缓了其对传统杀虫剂的抗性演化速度。但是,鳞翅目害虫对甲维盐等十六元大环内酯类杀虫剂抗性的适应性进化问题使该类杀虫剂对鳞翅目害虫的可持续控制作用面临重大挑战,已有抗药性相关报道证实小菜蛾对该类杀虫剂的抗性发展日趋严重。尹勇对部分地区甜菜夜蛾田间种群进行了抗药性监测工作,发现某些地区的甜菜夜蛾种群已对甲维盐产生低等到中等水平抗性。司升云等报道了宜昌地区甜菜夜蛾田间种群对甲维盐的抗性已达中等抗性水平。Che等也报道了部分甜菜夜蛾田间种群对甲维盐具有高水平抗性(上海及云南等地)。
2.甲维盐的抗性机理研究概况
现有研究认为,节肢动物和线虫对大环内酯类药剂,如阿维菌素,甲维盐的抗药性,大多数情况下与多个遗传因素有关。主要机制包括:代谢抗性,包括解毒代谢酶中的细胞色素P450单氧酶 (P450)、谷胱甘肽S-转移酶(GST)和酯酶(EST);减少杀虫剂的角质层渗透;靶标位点不敏感,如门控氯通道的构象变化;细胞膜上三磷酸腺苷结节盒转运蛋白 (简称ABC转运蛋白,ATP-bindingcassette transporter,ABC-transporter)在phase III的解毒过程中,ABC转运蛋白可以主动将细胞内的有毒物质泵出细胞,有助于昆虫抵抗异生物质。
2.1 解毒代谢酶抗性
研究人员认为甲维盐的作用机制与其类似物阿维菌素相似或相同,也可由多功能氧化酶活性的变化引起。郭炜通过增效剂试验证实了稻纵卷叶螟解毒代谢酶对甲维盐的解毒代谢作用,说明解毒代谢酶活性的变化可能导致稻纵卷叶螟对甲维盐抗性的形成。有报道通过增效剂试验证明小菜蛾对阿维菌素抗性与多功能氧化酶相关,同样的结果也在马铃薯甲虫中有所发现。还有研究发现,三大解毒代谢酶的活性变化是西花蓟马对甲维盐产生抗药性的主要原因。
2.2 靶标抗性
赵卫东等报道,乙酰胆碱酯酶活性变化是导致二斑叶螨对阿维菌素产生抗药性的重要原因之一,同样的结果在西花蓟马甲维盐抗性种群中也得到了验证。但是,乙酰胆碱酯酶活性的改变作为昆虫对阿维菌素类杀虫剂抗药性机理的报道较少。
大多数研究仍认为该类药剂是作用于半胱氨酸换配体门控离子通道家族基因,通过破坏寄生虫神经肌肉系统达到杀虫目的。在初的研究中,并不知道寄生虫存在谷氨酸门控氯离子通道(GluCls),大环内酯类杀虫剂的作用靶标被认为是GABA受体。大约10年后,在秀丽隐杆线虫中克隆出2个GluCl亚基,并在非洲爪蟾蜍卵母细胞中成功表达。这2个亚基能够形成对谷氨酸、鹅膏蕈氨酸盐、伊维菌素和其他阿维菌素类敏感的杂聚肽通道。Etter等认为α亚基可以为谷氨酸提供1个结合位点,但是不能打开离子通道。GluClα1基因在咽肌细胞pm4、pm5 和 一 些 神 经 中 表 达 ,GluClβ 在 pm4 中 表 达。Vassilatis等发现伊维菌素和谷氨酸均能降低谷氨酸受体的敏感性,点突变可导致结合能力下降。
在非洲爪蟾蜍卵母细胞中表达捻转血矛线虫的GluCl亚基,该亚基被伊维菌素和莫昔克丁缓慢的不可逆转的激活。尽管GluCl作为靶标位点似乎被更广泛的接受,然而,人们普遍认为,阿维菌素类药剂对GABA和GluCl都起作用。Arena等的研究发现:阿维菌素和米尔贝霉素可以与线虫GluCl结合并激活,表明GluCl是阿维菌素和米尔贝霉素在线虫的主要靶标位点。伊维菌素对捻转血矛线虫GluCl具有高亲和力,进一步证明这种受体是伊维菌素在线虫的靶标位点。其他阿维菌素类药剂与伊维菌素在GluCl上的结合位点相同,但是其亲和力相对较低。苦味毒、氟虫腈和谷氨酸与GluCl通道上的其他位点结合。伊维菌素可不可逆转地激活秀丽隐杆线虫GluClα和GluClβ通道以及果蝇GluCl通道,但是伊维菌素无法与捻转血矛线虫和秀丽隐杆线虫的GluClβ亚基相结合,表明线虫GluClα亚基对药物具有选择性。使用抗-HcGluClα/β和抗-GABA抗体,HcGluClα和β亚基定位在捻转血矛线虫GABA运动神经元,进一步证明这2个亚基构成受体的形式。用特定的抗体定位捻转血矛线虫GluCl3α,发现其定位在线虫的主要化学感觉器官-头感器。上述研究结果均可证明GluCl及GABA是大环内酯类药剂的主要作用靶标。
2.3 ABC转运蛋白诱导抗性产生
ABC转运蛋白作为超家族跨膜蛋白,从原核生物到人类均保守存在,基于序列的相似性,这些蛋白被分为8个亚家族,用A~H表示。这类跨膜蛋白不仅可以转运多种底物,还有其他作用,如细胞信号和核糖体的组装和翻译。现有研究认为ABC转运蛋白可以将毒性物质经过初级和次级代谢(PhaseⅠ和Ⅱ)形成的极性产物或螯合物强制性排出胞外(Phase Ⅲ),有时候ABC转运蛋白还能直接将有毒物质排出胞外 (Phase 0),ABC转运蛋白这种排出作用可减少胞内药物的积累,实现解毒,导致耐药性产生。据报道,ABC转运蛋白与27种分属不同种类的杀虫或杀螨剂的抗性有关,主要是ABCB、ABCC和ABCG 3个亚家族的基因,既有基因突变造成与底物亲和力下降,也有增加表达量引起对药物或其代谢产物的排出作用增强。
随着研究的深入,有证据表明ABC转运蛋白可以吸收、结合和消除宿主和寄生虫中的大环内酯类药剂,其中包括P-glycoproteins (P-gps,ABCB1)。1976年首次在仓鼠卵巢细胞中发现P-glycoproteins,其由MDR/ABCB1编码。其在保护组织免受有毒异物和内源性代谢物伤害中起着至关重要的作用,也影响许多重要药物的吸收和分布。P-gp的底物广泛且具有特异性,阿维菌素类药剂,如甲维盐、伊维菌素均是其底物。P-gp被证实参与了许多寄生虫和昆虫对阿维菌素类杀虫剂的抗药性形成。此外,P-gp的过量表达已导致多种昆虫产生抗药性种群,如二斑叶螨、鲑鱼海虱、烟草蚜虫。
使用ABC转运蛋白抑制剂维拉帕米处理鲑鱼海虱和昆虫,均证实ABCB HTs/P-gp可通过协同作用抑制大环内酯类的毒性。用大环内酯类药剂处理人类体虱、海虱成虫和小菜蛾均可诱导ABC转运蛋白表达上调,其中甲维盐/阿维菌素处理海虱成虫/小菜蛾导致其ABCB FT/P-gp表达量上调。Okechukwu通过ATPase活力测定以及竞争性抑制试验证明了甲维盐与ABC转运蛋白相互作用,大多数的大环内酯类药物可刺激ABCB FT/P-gp介导的Rhodamine 123流出,通过剂量-时间方式诱导ABCB FTs/P-gp表达,直接激活钙离子通道,间接的激活氯离子通道提高胞内钙水平。使用RNAi敲减在人类体虱中上调表达的ABC转运蛋白基因验证其功能,发现这些基因在对伊维菌素的代谢及抗药性产生中起到了至关重要的作用。这些发现均表明,阿维菌素/甲维盐是P-gp的底物,能诱导ABC转运蛋白表达增加,P-gp mRNA表达量的增加可能导致阿维菌素类药剂的有效性降低。
结 语
综上,昆虫对甲维盐的抗药性机理是复杂的,不同昆虫种群的抗药性机理也不尽相同,因此研究昆虫对甲维盐的抗性机理可为科学合理地使用该类杀虫剂,延长产品寿命提供重要的科学依据。甲维盐可与其他多种不同作用机理的杀虫剂进行混用或轮换使用,以延缓昆虫对其抗药性的产生及发展。在部分阿维菌素类药剂抗性水平较高地区应立即停用或暂缓使用该类药剂,等到该地区对阿维菌素类药剂抗性水平下降再重新策划使用方案,以防田间害虫抗性基因频率增加,丧失该类药剂对害虫的可控力。




