背景及概述[1]
3,4,5-三甲氧基溴可用作医药合成中间体,可由5-溴-1,2,3三羟基和二甲酯反应制备,也可由4-溴-2,6-二甲氧基酚作为反应原料制备。
制备[1-2]
方案一、
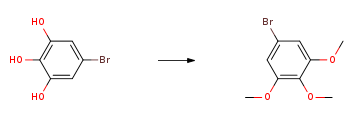
将5-溴-1,2,3三羟基(1.3g,5.63mmol)、1MNaOH(14mL)和二甲酯(800μL,加入16.89mmol)的混合物冷却至10℃。将该混合物加热回流3小时,然后加入另一份二甲酯(800μL)。将混合物在回流下再加热3小时,将混合物冷却过夜,并将灰色固体滤出,然后将其溶于50mL中,用5%NaOH-H2O,水,盐水洗涤,然后干燥(MgSO4)并浓缩,得到3,4,5-三甲氧基溴(1.39g,76%)。1HNMR(CDCl3)δ6.72(s,2H),3.85(s,6H),3.82(s,3H);m/z。13CNMR(CDCl3)136.67、137.11、115.92、108.07、60.58、56.05。
方案二、
将74g(0.32mol)的4-溴-2,6-二甲氧基酚和32g(0.8mol)的NaOH在850ml H2O中的混合物冷却至10°C,然后添加45ml(0.48mmol)的二甲酯,将混合物回流3小时,然后加入等量的二甲酯(总计0.96mol)。将混合物再回流3小时,冷却过夜后,灰色产物固化并滤出并溶于1.21中,过滤溶液以除去不溶的杂质,并依次用5%的NaOH溶液(200ml),水(2×200mL)和盐水(200mL)洗涤。醚相经Na2SO4干燥,得到灰白色固体,将其在己烷(300ml)中重结晶,得到62.3g(79%)的3,4,5-三甲氧基溴。
参考文献
[1]US2003176478
[2] CN01819067.7邻位取代的手性膦和三价膦酸酯及其在不对称催化反应中的用途




